重磅炸弹来那度胺化合物专利中美欧命运比较
作者 | xiaoxuer
(本文系知产力获得独家首发的稿件,转载须征得作者本人同意,并在显要位置注明文章来源。)
(本文6872字,阅读约需14分钟)
来那度胺化合物由来
说起来那度胺,不得不提到20世纪50年代医学史上的巨大灾难-反应停事件。反应停也叫沙利度胺,是一种致畸药物,20世纪50至60年代初期在全世界广泛使用,它能够有效地阻止女性怀孕早期的呕吐,但也妨碍了孕妇对胎儿的血液供应,导致大量“海豹畸形婴儿”出生。因此沙利度胺被禁用了40多年。但是,科学家们并未放弃对沙利度胺的深入研究,经研究发现其在免疫、抗炎、抗血管生成等方面有一定的作用,并于1998年,经美国FDA批准其上市用于治疗麻风性结节性红斑,之后又发现沙利度胺可以治疗多发性骨髓瘤。但是沙利度胺的致畸作用仍然限制着它的应用,因此科学家为了减少其不良反应,科学家开始研究与沙利度胺结构相似的衍生物,于是便有了来那度胺。

药品名称:来那度胺(Lenalidomide)
商品名:瑞复美(Revlimid)
化学名:3-(4-氨基-1-氧代-2- 异吲哚啉)哌啶-2,6-二酮
研发公司:美国赛尔金(Celgene)公司
上市:2005年12月,美国
主要适应症:骨髓增生异常综合征(MDS)、多发性骨髓瘤(联合地塞米松)、套细胞淋巴瘤(MCL)
分子结构:
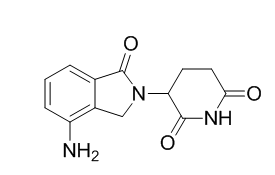
来那度胺自2005年上市后,就不断拓宽其适应症,销售额也是一路飙升,2015年已突破了50亿美元,2016年接近70亿美元,据汤森路透数据推测,预计2019年其销售额将突破百亿美元,可以看出来那度胺市场空间庞大,将成为超级重磅炸弹药物。
来那度胺化合物专利中美欧命运比较
制药领域的专利大致可分为化合物(通式化合物、晶型、制剂、前药、衍生物、活性代谢物、中间体、杂质)专利、用途专利、工艺专利等等,而其中化合物专利中的通式化合物专利可以说是核心中的核心,因为相对于其他专利来说通式化合物专利具有侵权可判定性强、稳定性高、难于规避等特点,因此各制药企业对于通式化合物专利的重视程度也就不言而喻了。但是由于管理、成本、市场等多方面的因素,制药企业提交的专利申请文件习惯于按照本土国家的审查标准或实践经验来撰写,这就导致相同的申请文本有可能在不同国家的稳定性却不尽相同,下面介绍来那度胺通式化合物专利在中国、美国和欧洲的情况。
1,来那度胺化合物中国专利信息
专利号:CN97180299.8
申请日:1997.07.24
优先权1: 1996.07.24,US08/690,258
优先权2: 1996.08.22,US08/701,494
优先权3: 1997.05.30,US60/048,278
授权公告日:2003.08.06
授权的权利要求书包含4个独权,权1为通式化合物权项,具体如下:
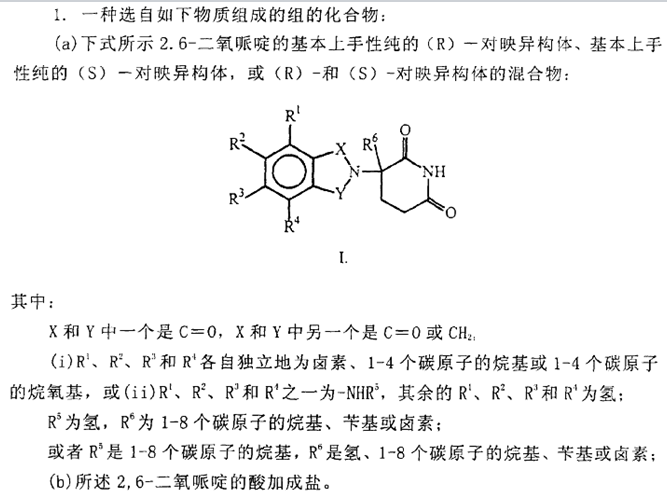
权2-9为权1的从属权项;
权10和权12为制药用途权项;
权11为组合物权项。
来那度胺化合物专利CN97180299.8在中国经历了两次无效,两次行政诉讼,最终结果为权利要求被全部无效,具体无效诉讼历程如下:
第一次复审委无效:
2008年12月8日,无效宣告请求人杜兆东,无效理由仅为权利要求1相对于证据1(“Structural Modifications of Thalidomide Produce Analogs with Enhanced Tumor Necrosis Factor Inhibitory Activity”,George W. Muller等,Journal of Medicinal Chemistry,Vol. 39 No. 17,第3238-3240页)不具备创造性;具体理由如下:
1)证据1的公开日为1996年8月16日,晚于本专利的最早优先权日(1996.07.24,US08/690,258),但是早于第二优先权日(1996.08.22,US08/701,494),由于US08/690,258中未记载本专利权利要求1的技术方案,从而权利要求1的技术方案不能享受US08/690,258的优先权日(1996.07.24),因此可以用于评价本专利的创造性。
2)证据1公开了权利要求1通式I结构类似的化合物,两者的区别仅在于证据1通式中与吲哚环相连的环为取代的苯环,本专利的通式中的该部分结构为取代的二氢哌啶环,上述结构区别是本领域技术人员容易想到的,且都具有TNFα抑制作用,而且本专利权利要求1也没有产生预料不到的技术效果,因此本专利权利要求1相对于证据1不具备创造性,不符合专利法第22条第3款的规定。
专利权人认为证据1通式中与异吲哚环相连的环为取代的苯环,本专利的通式中相同位置为二氢哌啶环,两个通式没有相同的基本核心部分或基本环,因此结构不接近,从而本专利权利要求1的化合物具有创造性。
2009年3月31日复审委员会对本案进行了口头审理,双方当事人充分陈述了各自的意见。专利权人当庭删除权利要求1并提交了意见陈述书,由于请求人的无效理由仅为权利要求1相对于证据1不具备创造性,在专利权人删除了权利要求1的情况下,复审委无需进一步审理其他权项,因此,复审委作出第13179号决定,维持CN97180299.8专利权有效。
本次无效,请求人为个人,请求无效的权项只有一项,无效的证据也只提供了一个,笔者猜测,无效请求人可能是试探性的看看无效的可能性吧。专利权人似乎也并未多花费时间和精力,口审时直接删除了权1。
第二次复审委无效:
2012年11月14日无效宣告请求人南京卡文迪许生物工程技术有限公司向复审委提交了无效请求,请求宣告涉案专利全部无效。其理由是:1)涉案专利说明书不符合专利法第26条第3款的规定;2)权利要求1-11不符合专利法第22条第3款的规定;3)权利要求1-11得不到说明书的支持,不符合专利法第26条第4款的规定。并最终因权利要求书不符合专利法第22条第3款规定,不具备创造性,该专利被宣告全部无效。
专利法第22条第3款规定,创造性,是同申请日以前已有的技术相比,该发明具有突出的实质性特点和显著的进步,该实用新型具有实质性特点和进步。
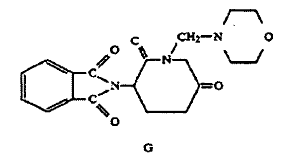
请求人提供了15份证据,其中主要证据6为PCT专利申请 WO9420085A1,其公开了化合物沙利度胺(thalidomide)和化合物EM-12 ,分子结构如下:
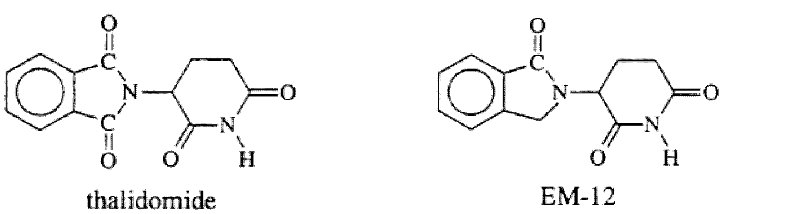
由上述结构可以看出来那度胺与EM-12的区别仅在于来那度胺在异二氢吲哚环的4位上具有氨基取代基,而EM-12的该位置是未取代的;
复审委认为,本领域技术人员在证据6已经公开EM-12的基础上,为获得结构类似、活性相当的替代化合物,有动机根据证据6通式化合物部分公开的内容在4位引入氨基取代基,这属于常规的结构修饰,是本领域技术人员解决获得替代化合物这一技术问题的常规技术手段,并且,由于该结构修饰非常简单,修饰后的化合物与已知化合物EM-12在结构上只有细微差异,因此,本领域技术人员可以预见,该结构修饰过程不会在实质上改变化合物的活性效果,即能够预料4位上氨基取代的化合物与未取代的EM-12具有类似的TNFα抑制活性。由此可见,由于本专利权利要求1保护的化合物与证据6中公开的EM-12结构十分接近,并且在证据6已经给出使用氨基进行结构修饰的启示的基础上,本领域技术人员在证据6的基础上获得本专利权利要求1的技术方案是显而易见的。因此,本专利权利要求1不具备突出的实质性特点和显著的进步,不具备专利法第22条第3款规定的创造性。
后续专利权人提交了补充实验数据,以证明本专利取得了预料不到的技术效果,克服了技术偏见并取得了商业上的成功,来证明本专利具备创造性。
对于专利权人提交的补充实验数据,复审委的观点是:1,该补充实验数据如果仅证明权利要求1化合物取得了一般TNFα抑制活性,则不需要补充,在判断创造性时已经予以认可;如果是用来证明权利要求1的化合物的技术效果明显优于EM-12,则由于本领域技术人员从原始申请文件中并不能获知该信息,则不允许补入;2,对于专利权人提到的证据6中的化合物比如EM-12具有致畸、胚胎毒性等毒副作用,以及苯胺具有致癌风险,而本专利化合物克服了技术偏见,对此,复审委认为一方面本专利说明书中并未有记载权利要求化合物不具有致畸作用,另一方面,已知化合物EM-12具有致畸副作用恰恰给出本领域技术人员对其结构进行修饰的动机;3,由于先申请制的原因,专利权人在后补充的关于本专利化合物效果的实验数据以及据此所得出的本专利取得预料不到的技术效果的结论并未记载在原申请文件中,因此不能用于证明本专利具备创造性。从而专利复审委作出第21646号决定,本专利全部权利要求均不符合专利法第22条第3款的规定,宣告全部无效。
另外,复审委强调:南京卡文迪许在请求书中同时提出本专利说明书公开不充分以及权利要求不具备创造性的无效理由,本决定是基于提供一种具有一般TNFα抑制活性的替代化合物这样的技术问题,认为现有技术已经公开了活性相同结构类似的沙利度胺和EM-12,由此可以预测本专利的来那度胺也具有一般的TNFα抑制活性,继而本专利说明书满足公开不充分的要求。如果专利权人坚持认为本专利解决的技术问题并不在于提供一般TNFα抑制活性的化合物,例如具有更小的致畸作用或者具有超出本领域技术人员可以预测的一般水平的TNFα抑制活性等其他预料不到的技术效果,则由于本专利说明书未记载任何实验效果数据,本领域技术人员根据说明书记载的内容并不能够确定本专利化合物具有这些技术效果,导致说明书公开不充分,不满足专利法第26条第3款的规定。
法院一审:赛尔金公司不服第21646号决定,向北京市第一中级人民法院提起行政诉讼。北京市第一中级人民法院认为:复审委关于第21646号决定结论正确,驳回赛尔金公司的诉讼请求。
法院二审:赛尔金不服原审判决,上诉至北京高院,理由是原审判决第21646号决定应适用1993年的《审查指南》,应接受后续补充实验数据。北京高院经过审理,认为原审判决认定事实清楚,适用法律正确,程序合法,应该予以维持。驳回上诉,维持原判。
2,来那度胺化合物美国专利信息
专利号:US5635517
申请日:1996.07.24
授权公告日:1997.06.03
授权的权利要求包含两个独权:权1和10。权利要求1为:The method of reducing undesirable levels of TNFα in a mammal which comprises administering thereto an effective amount of a compound of the formula:
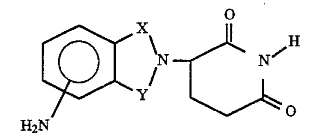
In which in said compound one of X and Y is C=O and the other of X and Y is C=O or CH2。
该权项虽然是method (用途) 权项,但是本领域技术人员都可以看出其保护力度跟通式化合物权项的保护力度相当。
权2-9为权1的从属权项;
权10为包含来那度胺化合物等在内的4个化合物。
IPR双方复审程序
美国的双方复审程序(Inter Partes Review,以下简称“IPR”)是依据美国法典35 U.S. Code Chapter 31于2012年9月16日生效的一个新的专利无效的诉讼程序,此程序在美国专利商标局专利审查与上诉委员会(以下简称“PTAB”)进行,IPR申请人只能根据美国专利法102和103法条对专利提出不具备新颖性或不具备显而易见性的无效请求。
该专利在2015年曾被第三方Coalition for Affordable Drugs VI (以下简称“Petitioner”) 以权利要求1-10不符合35 U.S.C.§ 103 (Condition for patentability; Non-obvious subject) 的规定为由提出IPR申请,Petitioner提出的具体理由有3个:
对比文件
法律基础
挑战权项
证据1:Anti-inflammatory immunosuppressive thalidomide analogs, 49 (4) INT’L J. of LEPROSY 511-512
证据2:US 5385901
§ 103
权1,7-9
证据:3:Structure activity relationship studies of thalidomide analogs as Anti-inflammatory and immunosuppressive agents, (4) INT’L J. of LEPROSY 512
证据4:WO9420085A1(中国第二次无效中的证据6)
§ 103
权2-6,10
证据5:NATIONAL TOXICOLOGY PROGRAM’S CHIMICAL SOLUBILITY COMPENDIUM (Lewis Publishers, Inc. 1992)
§ 103
权2-6,10
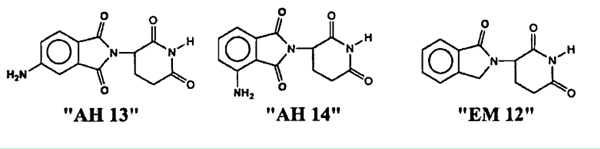
1)理由1,Petitioner认为证据2公开了EM12化合物,其具有TNFα抑制作用;证据1公开了苯环上具有氨基取代的AH13和AH14的化合物结构,AH13具有抗炎作用(anti-inflammatory),AH14具有免疫抑制作用(immunosuppressive);本领域普通技术人员应该容易结合证据1和证据2的教导去开发具有抗炎作用、具有免疫抑制作用或既具有抗炎作用也具有免疫抑制作用的沙利度胺类似物,并通过降低TNFα水平来有效治疗麻风结节性红斑(ENL,erythema nodosum leprosum)。因此Petitioner认为结合证据1和证据2本领域技术人员便可以得到苯环上氨基取代的沙利度胺类似物,并预期其具有抑制TNFα活性,因此,权利要求1和7-9在证据1和证据2的基础上是显而易见性的;2)理由2,Petitioner认为证据3和证据4结合,可以教导本领域技术人员对于在EM12苯环上进行氨基或羟基取代,既可以保留抗炎或免疫抑制的活性,又可以改变沙利度胺类似物的神经毒性和致畸毒性,因此具有启示作用;3)理由3,Petitioner认为证据5公开了EM12在水中是不溶解的,因此本领域技术人员为了改变EM12的溶解性,有动机引入供电子基团来提高溶解性,因此Petitioner认为权利要求2-6和10在证据3、证据4和证据5的基础上是显而易见的。
Petitioner同时还提供了专家证言(Dr. Heathcock’s Declaration)
专利权人初步回复如下:
第一,证据1仅讨论了麻风结节性红斑(ENL),并没有提到TNFα,也没有阐述具有麻风结节性红斑(ENL)的两个测试(anti-inflammatory或immunosuppressive)活性和TNFα抑制活性之间的关系;即使证据2教导EM12可能具有TNFα抑制活性,但并没有教导EM12对于治疗ENL是有用的。另外,EM12在抗炎测试中高剂量时也仅显示微小的活性,而低剂量时并没有显示具有抗炎活性和免疫抑制活性。所以证据2并没有给出本领域技术人员在治疗ENL时,可以通过使用具有TNFα抑制活性的沙利度胺类似物(如EM12)的教导;
第二,专利权人指出,证据2中也提到跟免疫相关的生物分子除了T-细胞TNFα以外还有细胞因子如IL-1,IL-6,IL-8,GM-CSF等;同时专利权人指出有些抗免疫药物,比如非甾体类药物在风湿性关节炎治疗时事实上增加TNFα活性水平的。因此不能证明免疫测试活性与TNFα抑制水平的相关性。
第三,证据2中的化合物G比EM12具有更好的TNFα抑制活性,因此EM12并非优选的化合物,本领域技术人员也不会选择EM12并结合证据1中的AH13和AH14来得到本专利化合物。
第四,专利权人认为化合物即使结构上的微小改变也会带来不可预期的活性改变,例如,证据1中的化合物AH13和AH14仅仅是苯环上氨基位置不同,结果却差别很大,AH13具有抗炎活性无免疫抑制活性,而AH14具有免疫抑制活性而无抗炎活性。
第五,专利权人还指出证据3、证据4、证据5也没有启示本领域技术人员去对EM12进行改构,也没有启示在沙利度胺类似物的苯环上引入氨基基团。
考虑了Petitioner的请求理由和专利权人初步答复后,PTAB认为Petitioner并没有阐述合理的理由以证明权利要求1-10中的任何一条权项在证据1-5的基础上是显而易见的。因此PTAB拒绝了Petitioner的IPR请求。
可以看出,在美国,PTAB对US5635517的创造性认可度较高,其专利权相对比较稳定。目前该专利正处于多家ANDA申报企业发起的PIV专利挑战中,笔者认为后续被无效的可能性比较小。
3,来那度胺化合物欧洲专利信息
专利号:EP0925294
申请日:1997.07.24
优先权1: 1996.07.24,US08/690,258
优先权2: 1996.08.22,US08/701,494
优先权3: 1997.05.30,US60/048,278
授权公告日:2002.12.11
授权的权利要求书包含3个独权,权1为通式化合物权项,具体如下:
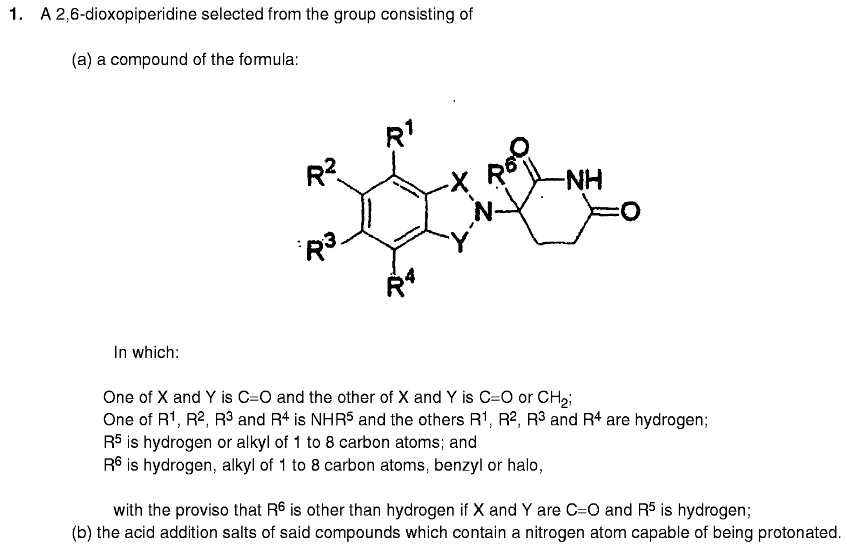
权2-3为权1的从属权项;
权4组合物权项;
权5为用途权项,权6为权5的从属权项。
该欧洲专利是通过PCT-EURO的途径进入欧洲的,在欧专局审查时,审查员有提到创造性问题,后续申请人通过提供补充数据,证明本发明的化合物比沙利度胺具有更优异的TNFα抑制活性,具有预料不到的技术效果,从而克服了创造性问题。授权后九个月的异议阶段无第三方提出异议;在各个国家生效后,也未检索到有第三方对该专利提出无效请求。所以笔者认为,在欧洲EP0925294的专利权也是比较稳定的。
经过以上来那度胺化合物在中美欧无效诉讼历程可以看出,同样是通式化合物专利,但是中美欧的命运却截然不同的,笔者分析原因为:
在中国,1)如果现有技术中给出了将发明技术方案与最接近的现有技术之间的区别特征应用于该最接近的现有技术以解决其存在的技术问题的启示,则该技术方案不具有创造性。如果所述的区别特征是本领域中解决所述技术问题的惯用手段,则可以认为现有技术中存在将该区别特征应用于最接近的现有技术中以解决其技术问题的启示。比如在本案中本发明与现有技术的区别特征为EM12苯环上的氨基取代,而氨基取代是本领域中解决所述技术问题的惯用手段,因此现有技术对于本发明是有启示的;2)不管是1993版的、2006版、2010版或是2010修订版的审查指南对于补交实验数据的规定都是一致的,必须遵守先申请原则:补交实验数据所证明的技术效果应当是所属技术领域的技术人员能够从专利申请公开的内容中得到的,在审查、无效、诉讼过程中提供的补充数据才可以被考虑。而来那度胺专利在说明书中的技术效果仅记载“式I化合物被用来抑制TNFα的不期望有的作用”以及“这些化合物还可以用于需要组织或抑制TNFα产生的人以外的哺乳动物的兽医治疗”,但并未给出任何活性实验数据,因此,本领域技术人员在阅读本专利说明书后,仅能够意识到本专利的化合物具有一般的TNFα抑制效果,而不会确信其具有超出常规水平的活性或者其他预料不到的技术效果。而关于降低了毒副作用、解决了现有技术致畸的问题,也没有在原始申请文件中有记载,因此后续补交的实验数据也是不予接受的。至于商业上的成功,由于不能证明是直接源于改进的技术特征、技术效果,一般也不予采纳。
在美国,1)审查员更注重现有技术对于本发明的技术方案是否有合理明确的启示,比如虽然本发明化合物与沙利度胺及上面提到的EM12结构非常类似,但是如果现有技术没有明确教导EM12及沙利度胺经过简单的官能团的取代、替换或改变可以得到本发明化合物,则不会影响本发明的非显而易见性;2)审查员对于申请日后补充的实验数据的接受程度是相对比较宽松的,即使在原始申请文件中没有具体的实验方法、实验数据,后续如果有新的证据证明其与现有技术相比具有预料不到的技术效果,降低了副作用或者克服了技术偏见,甚至是商业上的成功,都可能被采纳,很明显专利权人后续证明来那度胺在TNFα抑制活性上与现有技术相比具有预料不到的技术效果,解决了沙利度胺致畸的问题,而且从不断拓宽的适应症,节节攀升的年销售额可以看出,商业上也是非常成功的,因此PTAB没有接受第三方的IPR申请。
在欧洲,对于结构类似的化合物,现有技术对于后续发明的启示的判断标准跟中国较类似,但是对于申请日后补充数据的接受程度又跟美国较为相似。
启示
对于专利申请人来说,在专利申请前就应该对现有技术了如指掌,专利撰写时应提前规划好权利要求书的布局,清楚的在说明书中记载实施例的合成方法、化合物的表征、生物活性测试方法及效果数据,特别是相对于最接近的现有技术具有优势的效果数据,以经得起在各个国家的审查、无效和诉讼的考验。比如,假设来那度胺化合物专利的原始申请文件中有记载TNFα抑制活性数据或者降低毒副作用的数据,则在中国该专利的稳定性会大大增加。
对于仿制药企业来说,在项目的立项之初即需要对现有技术进行全面的检索分析,提前做好障碍专利应对策略,实时监控和分析,依据研发的进度及无效诉讼的周期适时的对障碍专利发起挑战,为提前将产品推入市场做好准备。



















