金杜知卓 | 从恩扎卢胺化合物无效案看中国化合物专利结构非显而易见性和补充实验数据问题

——评(2022)最高法知行终287号二审判决
作者 | 邰红 韦嵥 金杜律师事务所
编辑 | 布鲁斯
近日,最高人民法院知识产权法庭作出(2022)最高法知行终287号二审判决,撤销国家知识产权局第37674号无效决定,认定恩扎卢胺化合物专利ZL200680025545.1具有创造性。至此,自2018年起关于恩扎卢胺化合物专利的专利无效争议得到了终审裁判,宣告该专利无效的两项专利无效决定37674号和38507号决定分别被北京知识产权法院(2019)京73行初7080号和最高人民法院(2022)最高法知行终287号两件生效判决撤销。
特别地,在二审判决中最高人民法院认定恩扎卢胺的结构非显而易见性,且接受了专利权人在行政诉讼阶段提交的补充实验数据并依据补充实验数据认定了恩扎卢胺具有预料不到的技术效果。据笔者所知,本案是首个接受补充实验数据并依据该数据确认技术效果的专利确权行政案件,具有高度典型性。在此,笔者以本案代理律师角度,梳理本案的审判过程,以供读者参考。
一、背景简介
本案针对的化合物如下式所示,即涉案专利ZL200680025545.1中的RD162',也称为恩扎卢胺。
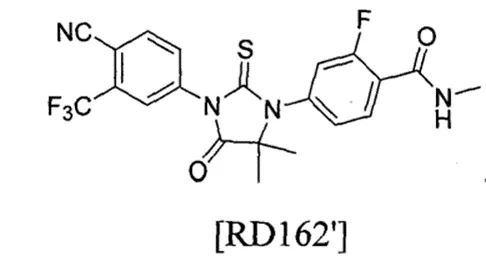
恩扎卢胺是第一种可延长去势抵抗性前列腺癌(CRPC,也称为激素难治性前列腺癌,HRPC)患者总生存期的抗雄激素药物。前列腺癌是第二大常见男性恶性肿瘤,也是癌症死亡的主要原因。从历史上看,治疗晚期前列腺癌的方法包括放射疗法、细胞毒性化疗和雄激素剥夺疗法,如手术去势、雌激素疗法、促性腺激素释放激素疗法和使用抗雄激素药物。然而,尽管雄激素水平处于去势水平,前列腺癌最终仍会进展(称为CRPC/HRPC的状态),原因尚不清楚。在优先权日之前,化疗药物Taxotere®(多西他赛)是第一种可延长转移性CRPC(mCRPC)生存期的治疗方法。然而,它提供的益处中等,存在明显不良副作用,部分患者无法耐受或者仍然可能发生进展。
恩扎卢胺与之前批准的抗雄激素药物相比,临床前和临床特性均有显著改善。由于在去势抵抗性前列腺癌(CRPC)治疗中的优异性能,2012年FDA批准Xtandi®(恩扎卢胺)用于治疗既往接受过多西他赛化疗的mCRPC患者,审评仅用时3.3个月。安可坦®(恩扎卢胺)被国家药品监督管理局药审中心确定为优先审评药物,并于2019年11月获国家药品监督管理局批准。
在原研药在中国获得上市许可之前,已有请求人向国家知识产权局原专利复审委员会提出无效宣告请求。国家知识产权局分别于2018年11月和2019年1月分别作出第37674号和第38507号无效决定,认定涉案专利不具有创造性,宣告涉案专利全部无效。
二、无效决定总结
两项被诉决定中,引用WO2006/028226A1中的化合物31和化合物41作为最接近的现有技术,其结构与恩扎卢胺记载如下。
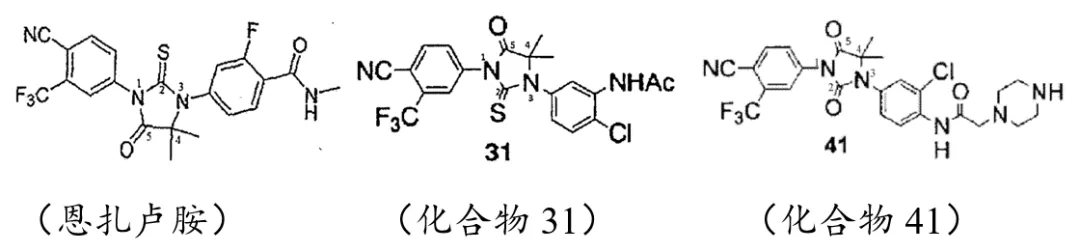
针对技术效果和实际解决的技术问题,无效决定认为,本专利只在图21A和图21B中记载了恩扎卢胺的体外活性数据,而两者存在实验数据矛盾。涉案专利也没有记载实验数据可以证明恩扎卢胺的活性高于化合物31或化合物41。因此,被诉决定认为实际解决的技术问题是提供另一种活性种类相同的替代化合物以治疗前列腺癌。
针对技术启示,无效决定分别引述US5411981或CN1049214C,认为上述化合物31/41与恩扎卢胺均具有苯环-咪唑环-苯环相连的三环结构,均落入US5411981或CN1049214C的通式定义范围内,也可以推知该结构为共同的结构,对活性种类不会有显著影响。此外,结合生物电子等排体理论和基团反转理论,存在对结构进行修改的动机和启示。
综上,无效决定认定恩扎卢胺相对于现有技术不具有创造性,宣告涉案专利全部无效。
三、一审判决总结
专利权人不服无效决定,向北京知识产权法院提起行政诉讼。在行政诉讼程序中,专利权人委托第三方进行了补充数据,并提交了第三方出具的恩扎卢胺、化合物31、化合物41以及对照化合物比卡鲁胺在LNCaP/AR前列腺癌细胞动物移植瘤模型的体内抗肿瘤药效研究报告,该实验模型与说明书中记载的实验方案基本相同。
2021年12月,北京知识产权法院作出(2019)京73行初5353号和(2019)京73行初7080号一审判决,分别撤销两件无效决定,认定恩扎卢胺具有创造性。
关于最接近的现有技术的选择
一审判决认为虽然化合物31和化合物41是现有技术中较差的化合物,但研发人员选择研发起点时,并非仅会考虑效果最好的那部分化合物,因此化合物31和化合物41虽然并非最优选的研发起点,但本领域技术人员不会将其排除在可选范围之外。
关于技术效果和补充实验数据
一审判决认为说明书中仅在图21A和图21B中记载了拮抗效果,其与补交的实验数据所测试的动物体内实验的肿瘤大小变化数据并非必然对应,因此认定专利权人补交的实验数据无法证明恩扎卢胺相对于化合物31或化合物41具有更好的高拮抗低激动AR活性。
关于技术启示和结构非显而易见性
一审判决认为需要依据客观真实的研发规律进行判断。尤其应当注意的是,在这一过程中,因涉案专利的化合物尚未出现,本领域技术人员并不知晓与现有技术之间的区别技术特征,因此本领域技术人员并不会直接着眼于区别技术特征进行研发。
一审判决还认为,依据通常研发规律,本领域技术人员会面临多种修改选择,具体包括基本结构是否需要修改,如果修改,应当如何修改,取代基是否需要替换,哪些位置的取代基需要替换等等。因此,显而易见性的判断需要关注上述每一个环节。
一审判决进一步认为,根据现有技术,本领域技术人员并非必然会选择区别技术特征所对应的位点进行特定的取代基的替换。无效请求人没有结合所涉AR配体领域给出替换的位点和基团的合理说明或者提交相关证据。对于生物电子等排体,规律性是相对的,不能仅仅因为存在该规律便当然认定其在各个药物研发领域具有普适性,仍然需要结合具体药物领域的构效关系敏感性等因素进行详细说明。对于US5411981或CN1049214C的通式记载,不能仅仅因为其记载的范围内包括了该取代基便当然认定其已给出相应教导。
最后,一审判决认为,创造性的判断主体应当是本领域技术人员,但具体案件中法官和审查员难以充分知晓真实的研发过程和研发规律,因此需要双方充分举证。对于已授权的化合物专利,尤其是已有上市药物的化合物专利而言,药品上市过程本身的复杂性及上市这一结果均已一定程度上验证了专利的技术效果。在此情况下,如果无效请求人仍然认为涉案化合物专利应予无效,应当承担更多的举证和说明责任,以避免在案件中出现低估专利权人创造性劳动的后果。
综上,一审判决认为请求人未给出充分理由和证据说明本领域技术人员无需创造性劳动即可获得恩扎卢胺,因此认定恩扎卢胺相对于现有技术具有创造性。
四、二审判决总结
针对(2019)京73行初5353号一审判决,一审第三人(请求人)不服一审判决中关于非显而易见性的认定,一审原告(专利权人)不服一审判决中不接受补充实验数据的认定,均上诉至最高人民法院。
2024年4月,最高人民法院北京知识产权法院作出(2022)最高法知行终287号二审判决,部分更改了一审判决的认定,维持一审判决结论,认定恩扎卢胺具有创造性。
关于补充实验数据是否可以接受
二审判决认为,关于补充实验数据的接受,需要满足积极条件和消极条件,即原专利申请文件应当明确记载或者隐含公开了补充实验数据拟直接证明的待证事实,以及不能通过补充实验数据弥补原专利申请文件的固有内在缺陷。具体到本案中,
第一,关于涉案专利记载的技术效果,说明书已经明确记载了其目的为“提供用于治疗激素难治性前列腺癌(HRPC)的新化合物”,而恩扎卢胺属于1类化合物,且记载了“1类化合物(表5)在治疗前列腺癌中与比卡鲁胺相比要好很多”,“1类化合物在用于作为AR拮抗剂以及在激素难治的前列腺癌中作为治疗剂是特别有利的”。
第二,图21A和图21B的实验目的是表明恩扎卢胺显著优于阴性对照组溶媒载体,并且在低浓度下显示出剂量依赖性的抑制活性,可以表明该化合物存在有效性;结合涉案专利说明书整体记载,可以表明恩扎卢胺相对于溶媒载体和比卡鲁胺具有更高的高拮抗低激动AR活性;而其所谓实验数据矛盾的问题,最高人民法院考察了图21A和图21B的数据差异的成因,认为专利权人主张两组实验源于不同日期使用不同批次的细胞完成,从而作用强度差异存在差异的解释具有合理性。因此,在整体考察说明书公开内容的基础上,本领域技术人员可以理解,本专利说明书中已经公开了作为1类化合物的恩扎卢胺,相较于比卡鲁胺,是用于治疗HRPC的治疗剂特别有利的化合物,该技术效果已在说明书中记载。
第三,关于补充实验数据的证明目的,专利权人委托第三方机构提供的研究报告意图证明在本专利描述的相同动物模型中,恩扎卢胺显示出优于化合物41的技术效果。在撰写专利申请文件时,专利申请人无法预期化合物41会在无效宣告程序中被引用为最接近的现有技术。专利权人提交与本专利实验方法相同的补充实验数据,用以证明本专利说明书已经公开的本专利化合物的技术效果,且该技术效果相对于作为最接近的现有技术化合物41更为优越,以此补充证明本专利技术方案具备创造性,该证明目的具有合理性。基于证明目的及本专利说明书公开的恩扎卢胺的优异技术效果,专利权人通过补充实验数据并非用于弥补原专利申请文件的固有内在缺陷,故应当予以允许。
基于上述理由,最高人民法院认定补交实验数据应予接受。
关于补充实验数据是否具有证明力
二审判决认为,补充实验数据是按照涉案专利中公开的相同模型实施获得的。关于补充实验数据的证明力,
第一,补充实验数据的具体实验条件虽然与本专利说明书记载的实验方案略有差异,其中肿瘤接种的细胞数和实验起始的肿瘤体积存在区别,但其系由不同实验机构根据实际情况进行调整所致,不会影响结果的准确性,属于可接受的范围,不足以影响其证明力。
第二,补充实验数据与本专利说明书公开的技术效果具有密切关联性。本专利的体外实验和体内实验高度相关。体外实验是为了观察细胞培养皿中的抑制作用,而体内实验是为了观察真实动物模型中相同细胞系的抑制作用,但这两种实验结果的根源都在于本专利要求保护的化合物包括恩扎卢胺对于激素难治性前列腺癌具有强抑制作用这一技术效果。本专利中测试了恩扎卢胺的体外细胞实验中的活性,补充实验数据是使用相同的细胞系转入体内进行测试,可以合理证明体外实验也具有相同的效果。
第三,综合考虑补充实验数据及本专利说明书公开的内容,可以证明恩扎卢胺的技术效果优于化合物41。补充实验数据是化合物41和恩扎卢胺在动物模型中的直接对比数据,反映了恩扎卢胺的技术效果优于化合物41。
基于上述理由,最高人民法院认定,本领域技术人员根据本专利说明书的记载和针对恩扎卢胺以及其他化合物描述的数据等整体公开内容,能够确信恩扎卢胺属于1类化合物的技术效果的存在。补充实验数据证明在本专利描述的相同动物模型中,恩扎卢胺显示出优于化合物41的技术效果。在基础上,本专利相对于最接近的现有技术所要解决的技术问题是提供具有更好的高拮抗低激动AR活性效果的化合物。
关于结构非显而易见性
二审判决认为基于WO2006/028226A1、US5411981与公知常识的结合,本专利的化合物在结构上是非显而易见的。
第一,US5411981的通式并非所谓“苯-咪唑环-苯”三环结构,其实施例合成的化合物中均不具有所谓的三环结构,被诉决定认定该三环结构是从其通式I中定义中进行多层次且多选项的选择后得出的。此外,生物电子等排体原理仅仅是经验法则,不能在不考虑母核结构及构效关系的情况下普遍适用。
第二,本专利的化合物具有敏感的构效关系,对其活性的预见性差,根据本专利说明书中的记载,在乙内酰脲化合物的结构中看似微小的改变可以造成在治疗前列腺癌中化合物的性质发生很大的变化。
第三,基于上述两点,本领域技术人员为解决提供具有更好的高拮抗低激动AR活性效果的化合物这一技术问题,对于在WO2006/028226A1的基础上结合US5411981与公知常识得到本专利的化合物缺乏合理的成功预期。
综上所述,最高人民法院认定恩扎卢胺化合物相对于现有技术具有创造性。
五、典型意义
本案历经接近六年的无效确权争议,具有高度典型性。特别地,在本案无效决定和一审判决作出之后,其中对于补充实验数据的可接受性问题以及化合物结构非显而易见性等创造性判断的前沿问题,均在医药领域引发广泛讨论。最高人民法院的二审判决对这些前沿问题均进行了回答。
关于补充实验数据问题
补充实验数据问题一直以来是医药专利审查中的重点内容。特别是在说明书中未明确记载数据的情况下,是否可以通过补充实验数据证明相关技术效果已充分公开,或者相对于对比文件是否具有更优异的技术效果,是长期以来医药领域争议的焦点问题。
最高人民法院于2020年发布《关于审理专利授权确权行政案件若干问题的规定(一)》,第十一条规定了药品专利的申请人或专利权人可以在申请日以后提交实验数据用于进一步证明充分公开或者与对比文件不同的技术效果。国家知识产权局亦在2021年1月15日开始实施的《专利审查指南》的修改内容中进一步规定了补充实验数据的审查原则,并增加了两个具体的示例。
最高人民法院进一步在2020年作出(2019)最高法知行终33号中首次确立了更具体的判断标准,即需要满足“原专利申请文件应当明确记载或者隐含公开了补充实验数据拟直接证明的待证事实”的积极条件以及“申请人不能通过补充实验数据弥补原专利申请文件的固有内在缺陷”的消极条件。该案件也被选为最高人民法院知识产权法庭成立五周年100件典型案例之一,并多次选入最高人民法院知识产权法庭裁判要旨摘要。
此后,基于过去四年的专利授权确权案件的审查实践,国家知识产权局发布了《“申请日后补交实验数据”相关审查规则诠释》系列文章,北京知识产权法院发布了《补交实验数据与创造性判断》,各自结合案例阐述其审查审判思路,在业内引发高度关注。然而,在卡利拉嗪案、卢卡帕利案、司美格鲁肽案等多个专利无效案件中,国家知识产权局与北京知识产权法院对补充实验数据的实践审查标准仍然存在区别和差异。
在本案中,最高人民法院进一步明确了积极条件与消极条件的具体判断方式。针对积极条件,应当考察说明书的整体内容,包括结论性的文字描述、实验方案、实验数据、以及除了权利要求化合物之外的整体技术效果的记载,综合确定待证明的技术效果是否在说明书中明确记载。针对消极条件,专利权人提交的与本专利实验方法相同的补充实验数据,用于证明与对比文件相比更优越的技术效果,不属于弥补原专利申请文件的固有内在缺陷的情况。
此外,在考察专利文件记载的技术效果和补充实验数据的证明力时,在实际审查实践中,部分审查员要求专利文件中需要记载不存在任何差异的“完美数据”,并且要求补充实验数据的实验方案与说明书的记载“一字不差”,这实质上为补充实验数据的可接受性设置了不符合客观真实实验的过高要求,从而导致大多数补充实验数据难以被审查员接受。
对此问题,最高人民法院采取了更加求真务实的态度,并非采取机械判断的方式,而是从科学事实出发,实质性地考察说明书记载和补充实验数据所采用方案的合理性。针对说明书的记载的技术效果是否科学可信,最高人民法院综合考虑了图21A和图21B的实验数据所要证明的优异技术效果是相对于溶媒而言,即使作用强度因实验批次不同而存在客观差异,但剂量依赖性的趋势仍是不变的,从而认可本专利说明书记载的优异效果的科学性。针对补充实验数据的实验方案,最高人民法院并未要求补充实验数据必须与专利说明书中的实验方法完全相同,而是实际考察实验方案的区别是否会对结果准确性造成实质性的影响,进而判断补充实验数据的证明力。
笔者认为,最高人民法院在本案中进一步明确补充实验数据的可接受标准,有利于促进审查审判实践的统一一致,为医药行业的专利申请人和专利权人提供更明确的指导。此外,最高人民法院首次接受了补充实验数据并依据该数据认定涉案专利具有创造性,表明其对待补充实验数据更宽容、更灵活的审查态度。
关于结构非显而易见性问题
化合物结构的非显而易见性问题也是近年来医药专利审查中的重点问题。在实际审查实践中,部分审查员和代理人存在“唯效果论”的倾向,仅依据技术效果认定创造性,而对于化合物结构往往以“比大小、看位置、长得像”等模糊而主观的方式忽视化合物结构差异带来的非显而易见性。
对此,国家知识产权局在2020年十大复审无效案例(第45997号无效决定)和2021年十大复审无效案例(第48183号无效决定)等多个近期的无效案件中明确指出,应当结合现有技术整体教导,并结合具体药物领域的构效关系敏感性判断化合物结构,不应直接适用生物电子等排体等经验法则。最高人民法院在近期的(2021)最高法知行终846号中也同样明确认定结构差异显而易见需要与该类药物构效关系的现有技术作为证据支持,不能任意扩大生物电子等排体等概念的适用,该案件也被选为最高人民法院知识产权法庭成立五周年100件典型案例之一。
在本案中,最高人民法院再次明确现有技术的教导应当整体考虑,不能仅因通式在多层次的选项中涵盖了某一可能性就当然认定存在技术启示,也不能在不考虑母核结构及构效关系的情况下普遍适用生物电子等排体等经验法则。在本领域中客观存在敏感的构效关系的情况下,应当认为化合物结构的改变的预见性差,微小的结构改变均可能造成化合物的性质发生较大变化,从而认定不存在改变结构的合理的成功预期。
笔者认为,创造性判断过程的实质是对于真实研发过程的“虚拟”重构,即使在“三步法”中选择最接近的现有技术未必是发明人实际选择的发明起点,也应当在判断动机和启示时充分考虑真实的研发规律,综合考虑该领域的构效关系敏感性等因素判断,以避免出现《专利审查指南》中所指出的事后诸葛亮问题。本案进一步明确了该审查标准,表明了最高人民法院尊重客观研发规律,在创造性判断中以客观事实为基础的求真务实态度。
化合物专利是药物领域创新的基础专利,在化合物已经制成药物的前提下,这些化合物对人类社会有巨大贡献,属于专利法应当予以保护的发明创造。随着我国医药企业的创新能力的不断进步,加强医药领域的知识产权的保护不再仅是外国药企的呼声,而且也是国内医药企业的呼声。随着《专利法》第四次修改的正式实施以及药品专利链接制度、医药集中采购领域知识产权保护制度等多项制度的落地,我国已明确了保护医药知识产权、鼓励医药领域创新发展、优化营商环境的方针。最高人民法院在本案中进一步明确了补充实验数据的可接受标准,重申了化合物结构非显而易见性的重要地位,强化创新药企业对我国知识产权保护的信心,充分体现了在党中央和国务院制定的鼓励创新、保护知识产权的战略,值得业内充分关注和肯定。
联系作者

邰红
金杜律师事务所
知识产权部 合伙人
tinatai@cn.kwm.com

韦嵥
金杜律师事务所
知识产权部 律师
weijie@cn.kwm.com
(本文仅代表作者观点,不代表知产力立场)
图片来源 | 作者提供



















