从艾伯维与百济神州的专利战思考中国企业出海专利风险防控

作者 | 王欢 广东卓建(光明)律师事务所
编辑 | 布鲁斯
背景简介:
专利战背后的市场交锋
2023年6月16日国内创新药龙头百济神州发布公告,披露其自主研发的创新药泽布替尼(Zanubrutinib,中国商品名:百悦泽)在美国遭遇艾伯维(Abbvie)子公司起诉专利侵权,此公告一出立刻引发创新药企广泛关注。百济神州成立于2010年,成立初期就旨在“做最好的药”,短短几年时间百济神州已有3款创新药上市,其中涉案药品泽布替尼是最亮眼的一颗新星,根据百济神州公布的2023年上半年业绩快报,业绩同比增长30亿元其中有20多亿来自泽布替尼销售额增长。
本案涉案药品为一款BTK抑制剂小分子药物,BTK是B细胞受体信号通路中的关键组成部分,该激酶被激活是B细胞恶性肿瘤发生的重要驱动力之一。本案原告生产的伊布替尼(Ibrutinib)是首个上市的BTK抑制剂,自2103年11月上市至今获得了巨大的商业成功,2020年伊布替尼全球销售额达到82.13亿美元;2021年更是上升为97.77亿美元。百济神州研发的泽布替尼是第2代BTK抑制剂,2019年11月获美国批准上市,截止目前已在美国、中国、英国、加拿大等65个国际市场获批上市,根据百济神州公告披露,泽布替尼在头对头对比伊布替尼的临床试验中,在疗效、安全性等方面均优于伊布替尼。基于该结果,美国NCCN指南将伊布替尼从首选方案转移到了其他推荐方案,而泽布替尼从2A类优先推荐提升至1类优先推荐[1]。2022年伊布替尼的销售额首次出现下滑,百济神州的泽布替尼对于艾伯维伊布替尼的市场构成了非常直接的威胁。
伊布替尼的专利布局:
艾伯维的专利包围圈
在美国,医药领域的专利战数量排名第二,仅次于消费品领域,可以说,对于制药行业来说,专利诉讼几乎就是家常便饭,那些国际头部制药企业无不是专利战场中的老手[2],而本案原告艾伯维更是善用专利规则的高手,被业内戏称为“披着医药公司外皮的专利律师事务所”。
专利权人为伊布替尼编织了严密的专利保护网[3]:
• 化合物专利:2006年12月28日提交的正式申请,由于伊布替尼为新化学实体获得了320天PTE延长,该时间延长加在了专利US8008309上,此外,伊布替尼为儿童用药额外获得了6个月的PED独占期(该独占期可加在橙皮书所有专利到期日后面),因此该化合物专利到期日延长到了2028年5月13日,目前授权化合物专利的保护范围并不涵盖泽布替尼,该专利在30个国家或地区进行了布局,在美国的分案申请高达75篇,且仍有后续专利申请正在实审过程中。
• 适应症专利:适应症专利主要来源于3个专利族,第一个专利族来源于化合物专利分案分出的适应症专利,大部分是在2027年6月28日到期;第二个适应症专利族正式申请日为2011年6月3日,大部分专利到期日在2031年12月03日,该专利在21个国家或地区进行了专利布局,在美国的分案申请有22篇,本案艾伯维用于起诉百济神州的专利正是来源于该专利族的续案申请US11672803,该专利美国同族仍有后续专利申请正在实审过程中;第三个适应症专利家族正式申请日为2014年10月24日,通过增加剂量、区别适应症来获得授权,大部分专利在2035年4月24日到期,该专利在16个国家或地区进行了专利布局,在美国的分案申请有9篇,该专利美国同族仍有后续专利申请正在实审过程中。
• 晶型专利:2013年6月3日提交正式申请,目前橙皮书中包含4篇晶型专利US9296753、US9725455、US10106548、10125140,到期日最晚的是US9296753,到期日为2034年4月30日,该专利在36个国家或地区进行了布局,在美国的分案申请有26篇,该专利美国同族仍有后续专利申请正在实审过程中。
• 制剂专利:2013年6月3日提交正式申请,目前橙皮书包含4篇制剂专利US10294231、US10294232、US10752634、US10961251,到期日均为2033年12月3日,该专利在36个国家或地区进行了布局,在美国分案申请有26篇,该专利美国同族仍有后续专利申请正在实审过程中。
解密艾伯维专利埋伏战:
中美专利制度的巨大差异
艾伯维之所以能在专利战场上频频成功阻击竞争对手,一方面得益于其强大的研发管线和科研实力,另一方面得益于其善用专利规则,能将专利制度运用到极致,在本案中涉案专利US11672803专利保护范围本来并不包含泽布替尼的结构,当泽布替尼市场份额不断扩大时,艾伯维利用美国专利规则修改权利要求的保护范围,最终成功将泽布替尼划入专利的保护范围,专利授权当天,专利权人立即向法院提起专利侵权诉讼,对此很多国内的企业感到不解,艾伯维是怎么做到的,百济神州能提前预见到本起诉讼吗?想要解答以上问题,需要了解中美专利制度的巨大差异:
1. 主动分案制度的差异
分案申请可以分为申请人主动分案和根据审查意见进行的被动分案两种,在实践中,被动分案主要是为了审查员提出的单一性问题,而主动分案则在很多情况下与单一性无关,更多的是为了概括出不同的保护范围或争取更大的保护范围,但主动分案在中国的《专利审查指南》有诸多限制,能否主动分案需基于最早提交到国知局的原申请的法律状态,申请人必须在原申请被授权/被放弃/申请程序结束之前提交。在实务中,申请人进行分案后,经常会发现还需要对分案申请再作进一步修正或完善,此时就需要分出第二代乃至随后的多代申请。然而,由于此时原申请往往已经结案,根据现行分案规则,申请人已经无法继续分案[4]。
相较之下,美国的分案制度则更加灵活,只要有一篇专利处于未决(pending)状态,就可以以该专利为基础进行后续申请,美国的后续申请(Continuing Application)分为3种类型[5]:
(1)分案申请(Divisional Application):通常是审查员如果认为该专利申请权利要求主张了一项以上的独立发明,就会发出限制要求(Restriction Requirement)通知书,要求申请人把权利要求书限制为仅包含一项发明。对于从原申请中删除或撤回的权利要求,申请人可以提出分案申请。
(2)续案申请(Continuation Application):当母案申请中存在一些暂时无法获得授权但申请人又不希望放弃的技术方案时,申请人可以考虑CA。CA的说明书一般与在先母案的说明书保持完全一致,或者可以有微小调整,但不能含有任何新的主题,提出CA时,可以扩大权利要求的保护范围,但该扩大后的保护范围,应该能从说明书记载的内容得出,在实务中,申请人发现母案申请的权利要求保护范围过小,未能覆盖新产品或者竞争对手产品,可以基于母案说明书公开的范围修改权利要求,通过续案申请获得更大的保护范围,从而保持优势的市场竞争地位,本文涉案专利正是通过这种方式,将泽布替尼划入了专利保护范围。
(3)部分续案申请(Continuation-in-part Application):部分续案申请是重复母案申请的部分或全部实质内容,并且增加了在母案申请中未公开的内容。申请人可以随着产品迭代或技术更新,将新的发明主题通过部分续案申请提交,这种不确定性无疑给竞争对手形成更大的威慑作用。但需要注意的是,部分续案申请的新增发明主题无法享有母案相同的申请日,并且由于部分续案申请中涵盖新增发明内容的权利要求项的审查基准日是以新申请日为准,因而部分续案申请最好在母案公开前提出,如果是在母案公开后才申请的,母案或其同族可能成为现有技术文献,被用以驳回部分续案中新权利要求的可专利性。
2. 专利审查程序的差异
(1)主动修改的时机存在差异:在中国对于发明专利,申请人有两个主动修改时机,第一个时机是在提出实质审查请求时,第二个时机是在收到国家知识产权局发出的发明专利申请进入实质审查阶段通知书之日起的3个月,申请人可以对其专利申请文件进行修改,但是,对发明和实用新型专利申请文件的修改不得超出原说明书和权利要求书记载的范围,即不能通过主动修改扩大权利要求的保护范围。对于美国专利法而言,主动修改被称为“初步修改(Preliminary Amendment)”。初步修改的时机可以在PCT申请进入美国国家阶段的同时提出初步修改、在进入美国国家阶段的进入日之后的三个月内做出的初步修改,对于这两种情形提出的初步修改,只要该修改没有超出原始申请文件的记载范围,则审查员基本上无条件接受该初步修改,还有一种情况是在下发审查意见之前做出的初步修改,该种情形下只要初步修改不影响审查员已经基本完成的通知书准备工作或带来额外大量检索负担,则审查员也会接受[6]。本文涉案专利在审查意见下发前进行了3次主动修改,在修改过程中不断优化权利要求的保护范围。
(2)审查意见的答复机会不同:在中国专利进入实审阶段后,对于审查员的审查工作没有具体的时间限制,取决于案件的具体审查情况,一般而言在发出一通或二通之后,就可以做出驳回决定或授权通知书,而对于一些授权或驳回难度大的申请可能存在4次以上审通,但这种情况并不常见。因此申请人要非常珍惜每次答复的机会,权利要求修改的尺度很难把控,尤其是二通过后,如果修改不能满足审查的要求,随时面临被驳回的风险。在美国一般会下发Non-Final Rejection 和Final Rejection两次审查意见,专利申请被驳回后还可以通过RCE程序得到救济,申请人可以通过缴纳一定的费用重启审查程序,而且没有次数的限制,因此专利权人能够获得较多修改的机会,从而最终获得更加有利的保护范围。
(3)中美审查尺度存在不同:美国专利法对于说明书中披露的内容是否支持权利要求的门槛相对宽松,可以允许把说明书不同段落中披露的要素合在一起,来支持同一个权利要求的保护范围。在本案中,艾伯维在专利审查过程中将一个未在说明书中明确出现的化合物通式修改入权利要求中,属于“二次概括”,在中国专利法中是不被允许的。
上述差异体现了中国专利法更加注重维护公众预期利益,通过限制专利修改空间维护公众的行动自由空间。
涉案药品化学结构式
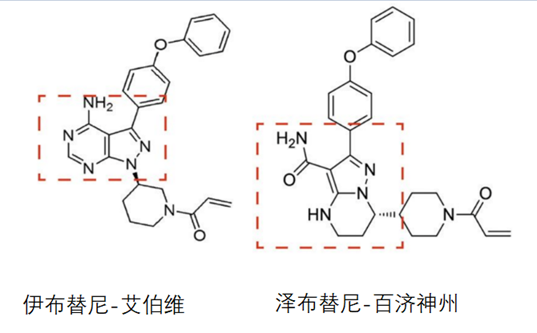
涉案专利US11672803的审查过程[7]:
2020-07-10专利权人提交涉案专利,起始权利要求保护范围较大,Btk抑制剂治疗疾病的方法;
2021-09-07第一次主动修改,修改后的权利要求限定了伊布替尼的具体结构及用量,范围很窄,此时权利要求还没开始靶向泽布替尼。
2022-02-18第二次主动修改,推翻了前面所有的权利要求,重新概括了一套权利要求,包含一个范围极大的通式,已开始涵盖泽布替尼。
2022-03-30专利权人进行了第三次主动修改,优化了表述形式。
2022-06-06审查员发出了Non-Final Rejection,认为权利要求范围太大,不能满足支持的要求。
2022-08-23 专利权人针对审查意见进行修改,大幅度收窄权利要求的范围,修改后的权利要求出现一个原说明书未出现过的通式,通式其他位置都是具体的限定,把上图红框位置定义为Z’, Z’为任意取代的稠杂环结构,这时候靶向泽布替尼的意图初现端倪。
2022-10-20 专利权人针对 Non-Final Rejection再次修改权利要求,其主要将Z’限定为包含2-4个氮杂原子的任选取代的稠合杂环系统。
2022-12-27 审查员发出了Final Rejection,审查员认为Z'的限定还是过于宽泛,包含2-4个氮杂原子的任选取代的稠合杂环系统可以有三个或者更多个环,并且环的大小也没有限于说明书的示例,所以得不到说明书支持。
2023-02-03针对Final Rejection进行了修改,修改后的的权利要求将Z'限定包含2-4个氮杂原子的任选取代的稠合杂环系统;其中任选取代的稠合杂环系统由包含至少一个氮杂原子的5元环稠合至包含至少一个氮杂原子的6元环组成;也就是我们目前看到的803专利的权利要求范围,从字面上看,泽布替尼似乎是落入了保护范围。关于Z’部分的支持,申请人指出专利说明书几个不同段落分别披露了heterocyclic ring、fused、ring system等要素,合在一起支持了权利要求结构中Z’部分的定义和整个结构[8]。
2023-02-28 审查员发出授予专利权通知书。
思考与启示:
中国企业出海如何防控专利风险
专利制度起源于欧洲,快速发展于美国,美国1790年颁布世界上第一部正式的专利法,我国于1984年颁布中国首部专利法,该法源于德国专利法体系并基于中国发展现状做了许多调整,40年来中国专利法做了四次修改,不断与国际及创新发展的国情相适应,与中国专利法相比,美国专利法更加复杂与灵活,对于深谙专利规则的跨国制药企业,专利战已然成为其阻击竞争对手的有利武器,在中国企业向全球市场迈进的过程中,势必要融入全球的价值体系和竞争体系。艾伯维与百济神州的专利纠纷给准备出海的创新企业敲响了警钟,笔者结合十余年医药知识产权研究经验做出如下思考:
1. 创新医药企业应针对核心产品加强国际专利布局的投入
随着国内医药企业创新实力及研发投入的不断增强,中国创新药行业正在经历一场多元化的创新革命,未来将会有更多的me-better(药物性能较以上是药物有显著优势)、first-in-class(首个针对某一靶点或具有全新作用机制的药物)出现,创新医药企业应打开国际专利布局视野:
1)提升专利撰写质量。中国专利一般10来页,20几页,而美国核心专利一般动则上百页,只有通过充分的描述,才能实现权利要求修改的更多可能性。
2)增加专利布局的数量与类型,从不同维度撰写出不同的保护范围,从而让专利保护更加立体。本案中可以看出艾伯维为涉案产品编制了严密的专利保护网,不同类型的专利申请有不同的节奏,与产品的研发上市的时间相配合,最大限度延长专利保护期限,核心专利家族的数量都在上百篇。
3)用发展的眼光看待专利布局。由于国际专利布局的成本较高,加之国内企业对于知识产权的重视程度不足,往往仅进行中国布局,或进行国际布局也只是聊聊几篇,很难达到灵活运用的效果。发明专利的保护期限一般约为20年,符合专利期限补偿的专利则能获得更长时间的保护,但专利申请的窗口期一般在1-3年左右,错过往往无法补救,企业家必须用发展的眼光去看待专利布局的问题,否则会面临“书到用时方恨少”的局面。
2. 建立专利侵权预警机制
医药企业在立项前往往会比较重视项目自由实施的风险,立项前对专利进行充分的调研,而忽视产品立项后专利信息的监控跟踪,专利信息的监控应该是持续的,从立项到上市一直持续到上市后,对于重点竞争对手、重点专利进行持续重点监控,评估潜在风险,提前做好预案。通过观察百济神州的专利布局,可以发现其对美国专利法是相当熟悉的,对竞争对手应该是有监控的,但艾伯维此次权利要求的修改能够获得授权,提前预判的难度确实很高,以事后诸葛亮的视角看待此事,如果当发现艾伯维做出权利要求修改向泽布替尼倾斜时,如果及时提交公众意见或异议,势必会对该专利的授权形成一定的障碍。
3. 认识到知识产权专业人才的重要性
医药领域的知识产权相对专业,如果仅通过外部代理所进行专利撰写,往往缺乏全局视野及相关专业背景,导致撰写质量无法保证。同时专业程度不够也无法做好专利信息监控,例如美国专利到期日的计算方法十分复杂,如果不懂美国专利法及医药领域相关制度,可能连专利的到期日都会算错。企业可以通过自身培养专业型人才或借助服务机构的专家,对企业的知识产权布局及风险防控进行专业管控。
注释
[1]手把手解密百济BTK被控专利侵权始末,作者秋春2021,2023年6月24日
[2]百济神州迎战全球“丛林法则”,发布于MedTrend医趋势,2023年7月13日
[3]U.S. FOOD&DRUG ADMINISTRATION Orange Book Orange Book: Approved Drug Products with Therapeutic Equivalence Evaluations (fda.gov)
[4]中国专利主动分案制度研究,发布于知产力,2017年12月4日
[5]涉外专利实务(美国篇),知识产权出版社,李钟主编,2021年10月第1版
[6]浅谈美国专利申请的主动修改,神仙谈专利,2019年11月5日
[7]Global Dossier Global Dossier - United States Patent and Trademark Office (uspto.gov)
[8]百济神州泽布替尼在美被艾伯维起诉专利侵权,辛筱斑,MedIP,2023年6月16日
(本文仅代表作者观点,不代表知产力立场)
图片来源 | 网络



















